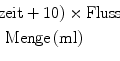, Dagmar Dohr2, Claudia Marks3, Martina Kahl-Scholz4 und Christel Vockelmann5
(1)
Praxis für Nuklearmedizin, Strassburger Allee 2-4, 45481 Mülheim, Deutschland
(2)
Christiansgasse 14, 8750 Glarus, Schweiz
(3)
Klinik für Radioonkologie, Universitätsklinikum Tübingen, Hoppe-Seyler-Str. 3, 72076 Tübingen, Deutschland
(4)
Möhnesee, Deutschland
(5)
Radiologische Klinik, Christophorus-Kliniken GmbH, Coesfeld, Deutschland
15.1 Allgemeines
M. Kahl-Scholz6
(6)
Möhnesee, Deutschland
15.1.1 Topographische Anatomie
Zu den anatomischen Strukturen des neurologischen Systems zählt das Gehirn mit seinen unterschiedlichen Anteilen, das Rückenmark sowie die Hirnnerven (Zentrales Nervensystem, ZNS) und die peripheren Ganglien und Nerven (Peripheres Nervensystem, PNS).
In der Bildgebung spielt vor allem die Darstellung des ZNS eine Rolle, daher wird sich hier auf die kurze Darstellung von Gehirn (Encephalon) und Rückenmark (Medulla spinalis) beschränkt.
Das Großhirn (Telencephalon) bildet den größten Teil des Gehirns und zeichnet sich strukturell durch die beiden Hälften (auch Hemisphären genannt), mehrere Furchen (Sulci) und Windungen (Gyri) aus. Weitere Anteile sind das Diencephalon (Zwischenhirn) mit dem Thalamus, Subthalamus, Hypothalamus, Hypophyse und Epiphyse sowie das Mittelhirn (Mesencephalum), Kleinhirn (Cerebellum), die Brücke (Pons) und das verlängerte Mark (Medulla oblangata), das in das Rückenmark übergeht. Die Grenze zwischen beiden letztgenannten Strukturen liegt etwa auf Höhe des Foramen magnum.
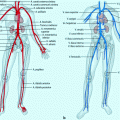
Das Gehirn wird durch zahlreiche Blutgefäße versorgt. Die vier Hauptarterien sind dabei die linke und rechte A. carotis interna sowie rechte und linke A. vertebralis. Die A. vertebralis bilden die A. basilaris, die wiederum im Schädelinneren den Circulus arteriosus cerebri speist (häufige Lokalisation von Aneurysmen etc.).
Gehirn und Rückenmark werden durch den sog. Liquor umspült, der durch den Plexus choroideus gebildet wird
Das Rückenmark ist ca. 45 cm lang und reicht bis zum 1./2.LWK. Es wird in die graue und weiße Substanz unterteilt, die unterschiedliche Nervenfasern führen. Vom Rückenmark gehen die Spinalnerven ab, die für die nervale Versorgung des Halses, Rumpfes und der Arme und Beine zuständig sind.
15.1.2 Funktion
Das Gehirn steuert alle wichtigen Funktionen, von der Motorik über die Sinnesempfindungen bis hin zu lebenswichtigen Prozessen wie Atmung, Herzschlag, Verdauung. Es ist ein kompliziertes System aus Neurotransmittern und -rezeptoren. Das Rückenmark stellt dabei sozusagen die Verbindung zwischen der zentralen Schaltstation „Gehirn“ und den anderen Körperanteilen wie Hals, Rumpf und Extremitäten dar.
15.2 Radiologische Diagnostik
C. Vockelmann7
(7)
Radiologische Klinik, Christophorus-Kliniken GmbH, Coesfeld, Deutschland
15.2.1 Sonographie
In der neurologischen Diagnostik spielt die Sonographie bei Erwachsenen nur im Rahmen der Gefäßdiagnostik (Kap. 14) eine Rolle. Das Gehirn ist von der Schädelkalotte abgeschirmt und entzieht sich einer sonographischen Untersuchung. Im Rahmen der Neonatalmedizin jedoch ist eine Sonographie des Neurocraniums durch die offenen Fontanellen, so nennt man die noch nicht geschlossenen größeren Lücken zwischen den Schädelknochen, sehr gut möglich. Hierdurch ist bei den kleinen Patienten eine nebenwirkungsfreie Untersuchung des Gehirns ohne wesentliche Vorbereitungen möglich.
15.2.2 Konventionelle Röntgendiagnostik
In der Diagnostik von Neurocranium, Myelon und peripheren Nerven spielt die konventionelle Diagnostik keine Rolle. Im Rahmen der Umgebungsuntersuchung z. B. zum Nachweis einer Spinalkanalstenose, von degenerativen Wirbelsäulenveränderungen oder auch zur Tumorsuche hat die konventionelle Röntgendiagnostik ihren Stellenwert in der Abklärung neurologischer Krankheitsbilder.
15.2.3 Durchleuchtung/Angiographie
Auch diese beiden Modalitäten dienen nicht der Untersuchung des Nervensystems selbst, sondern der Auswirkungen von neurologischen Erkrankungen oder zur Ursachenforschung. So führt z. B. ein Hirnstamminfarkt oft zu Schluckstörungen, die dann mit einer Hochfrequenzkinematographie („Schluckstudie“) näher klassifiziert werden, um eine adäquate Therapie einleiten zu können. Eine Myelographie dient zur Beurteilung einer Spinalkanalstenose und neuroforaminalen Engen.
Angiographisch werden die arteriellen und venösen Gefäße von Hirn und Rückenmark untersucht (Tab. 15.1). Hierbei werden z. B. Gefäßmalformationen untersucht, die zu intrazerebralen Blutungen führen können. Gleichzeitig ist hier oft eine minimalinvasive Therapie möglich, die an hochspezialisierten Zentren durchgeführt werden können.
Tab. 15.1
Diagnostische Angiographie A. carotis
Patientenvorbereitung | Aufklärung, Patienten entkleiden und ein Patientenhemd anziehen lassen; Leiste (Puls tastbar?) zur Punktion rasiert |
Positionierung | Rückenlage, steril abgedeckt, Punktionsstelle desinfiziert nach Hausstandard |
Material | 5000 IE Heparin i. A. Schleuse, Schleusenspülung, Diagnostik-Katheter (z. B. vertebralis), Diagnostik-Draht (z. B. Terumo-J-Draht[R]) |
Kontrastmittel | Pro Serie 6 ml iodhaltiges Kontrastmittel, Fluss: 8 ml/sec |
Einstellungen | Ap und RAO/LAO (im allgemeinen ipsilateral) |
Aufnahmekriterien | Karotisbifurkation vollständig aufgedreht und frei einsehbar |
15.2.4 Computertomographie
Die Computertomographie ist insbesondere bei einer akuten Klinik die bildgebende Untersuchungsmethode der ersten Wahl. Der große Vorteil im Vergleich zum MRT ist die Schnelligkeit und hohe Verfügbarkeit der Untersuchung. Zudem sind akut erkrankte Patienten häufig unruhig, sodass eine MRT-Untersuchung nicht gut durchführbar ist.
Mit Abstand die häufigste CT-Untersuchung ist in aller Regel die native Computertomographie des Kopfes (Tab. 15.2, Abb. 15.1). Hierbei geht es um die Beurteilung des Neurocraniums. Die Untersuchung wird mit gekippter Gantry erstellt; die Schichten entlang der Schädelbasis anguliert. Hintergrund hierfür ist, dass die Augenlinsen nicht im Strahlengang liegen sollen. Die Augenlinsen sind sehr strahlensensibel, und um eine vorzeitige Kataraktbildung zu verhindern, sollten Sie immer genau darauf achten, Ihre Untersuchung gut zu planen. Neuere Geräte können auch mit gekippter Gantry ein Spiral-CT anfertigen mit der Möglichkeit der multiplanaren Reformationen. Viele Geräte, die Sie in Ihrer Ausbildung und Ihrem Berufsleben bedienen werden, können das jedoch nicht. Daher werden hierfür noch sequentielle CT-Untersuchungen angefertigt.
Tab. 15.2
Untersuchungsprotokoll CT-Schädel
Patientenvorbereitung | Metall wie z. B. Hörgeräte, Schmuck etc. ablegen lassen |
Positionierung | Rückenlage in der Schädelschale, Kinn zur Brust nehmen lassen |
Scanbereich | Schädelbasis bis Schädelkalotte |
Röhrenspannung/-strom | 120 kV, zumeist feste mAS geräteabhängig |
Kontrastmittel | Nativ |
Reformationen | – |
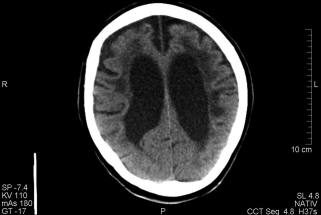
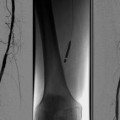
Abb. 15.1
CT-Schädel bei 53-jährigen Patienten mit multipler Sklerose
Da das Neurocranium von der Schädelkalotte so gut geschützt ist, ist leider auch immer eine erhebliche Dosis notwendig, um das Gehirn ausreichend beurteilen zu können. Diese Tatsache erkennen Sie auch an den Dosisreferenzwerten: hier liegen die Referenzwerte vom Kopf und dem gesamten Abdomen nicht weit auseinander.
Der Schlaganfall, also die Durchblutungsstörung des Gehirns, ist ähnlich wie der Herzinfarkt eine Erkrankung, bei der Zeit eine erhebliche Rolle spielt. Die Symptome eines Schlaganfalls sind z. B. die Schwäche einer Körperseite oder auch nur des Armes, Sprachstörungen und Verwirrung. Häufig tritt zusätzlich ein hängender Mundwinkel auf der gleichen Seite des Körpers auf. Auch Sensibilitätsstörungen der gleichen Körperseite oder eine Sehstörung gehören zu diesem Krankheitsbild. Ähnlich wie beim Herzinfarkt kann man den Patienten helfen, wenn Sie früh genug in die Klinik kommen. Noch wichtiger ist allerdings, dass dann auch in der Klinik die Abläufe optimal sind. Dazu gehört vor allem eine umfassende CT-Diagnostik der Erkrankung, die maximal 45 Minuten dauern sollte. Je schneller Sie allerdings mit der Untersuchung sind, desto wahrscheinlicher kann dem Patienten umfassend geholfen werden. Eine Therapie, die zumeist eine Lysetherapie , also eine starke Verdünnung des Blutes beinhaltet, kann zwar bis zu 4,5 Stunden nach Symptombeginn eingeleitet werden. Je eher die Therapie allerdings beginnt, umso mehr Nervenzellen können noch gerettet werden. Ein angekündigter „Lysekandidat“ sollte also dazu führen, dass Sie das CT freihalten und alles für die Untersuchung vorbereiten (Tab. 15.3). Zur Untersuchung gehören neben einer nativen CT des Schädels zum Ausschluss einer Blutung als Ursache für die Beschwerden eine CT-Angiographie der supraaortalen Gefäße mit intrakranieller Gefäßdiagnostik und oft auch eine CT-Perfusion. Die CT-Perfusion ist eine dynamische Untersuchung, bei der auf der gleichen Schicht (heute oft auch größere Anteile des Gehirns) über 1 Minute immer wieder Bilder aufgenommen werden, während Kontrastmittel durch den Körper fließt. Aus diesen Bildern kann man berechnen, wie stark die Durchblutung des Gehirns eingeschränkt ist. Mit den Ergebnissen der Untersuchung kann insbesondere in kritischen Fällen wie bei besonders alten Patienten besser entschieden werden, ob eine aggressive Therapie des Schlaganfalls sinnvoll ist oder nur unnötig risikoreich, ohne dass noch Gehirngewebe gerettet werden kann.
Tab. 15.3
Untersuchungsprotokoll CT-Lysepatient
Patientenvorbereitung | Röntgendichte Fremdkörper an Hals und Kopf entfernen |
Positionierung | Rückenlage, Kopf in die Kopfschale |
Scanbereich | Teil 1: natives Schädel-CT (Tab. 15.2) Teil 2: Perfusions-CT → Schicht auf Höhe der Basalganglien Teil 3: CT-Angiographie supraaortal (Trachealbifurkation bis Schädelkalotte) |
Röhrenspannung/-strom | Teil 1: 120 kV, feste mAs Teil 2: 80 kV, feste mAs (low-dose) Teil 3: 80–120 kV, Dosismodulation |
Kontrastmittel | Teil 1: nativ Teil 2: 40–50 ml Kontrastmittel, 50 ml NaCl; Fluss: 5 ml/sec Teil 3: 60–80 ml Kontrastmittel, 50 ml NaCl; Fluss: 4–5 ml/sec |
Reformationen | Teil 1: – Teil 2: Nachberechnung mit Perfusionsauswertung Teil 3: axiale 3 mm, coronar 3 mm MIP, sagittal 3 mm MIP |
15.2.5 Kernspintomographie
Für alle weiterführenden Abklärungen und auch die meisten planbaren Untersuchungen im neurologischen Bereich stellt die Kernspintomographie mit ihrem überragenden Weichteilkontrast die Untersuchungsmethode der Wahl dar (Abb. 15.2). Dabei ist jedoch immer wichtig, welche Klinik (also welche Symptome) der Patient aufweist. Es gibt zwar einige Sequenzen, die Sie nahezu bei jeder Kernspintomographie des Schädels anfertigen. Einige jedoch werden Sie nur messen, wenn der zuweisende Arzt eine entsprechende Frage formuliert. Ein Beispiel ist die Abklärung einer Ischämie (Tab. 15.4).
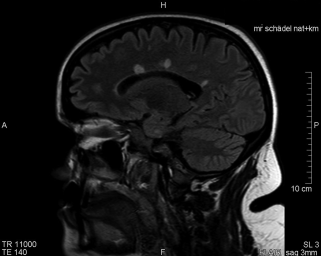
Abb. 15.2
MRT Schädel
Tab. 15.4
Untersuchungsprotokoll MRT Ischämie
Patientenvorbereitung | Sämtliches Metall, Scheckkarten, Schmuck etc. ablegen lassen |
Positionierung | Rückenlage |
Spule | Kopfspule |
Scanbereich | Gesamtes Neurocranium |
Sequenzen | Axiale T2 Flair, axiale T1w, sagittale T2w, axiale Diffusionswichtung mit ADC-MAP, axiale T2* |
Kontrastmittel | – |
Eine häufige Indikation insbesondere bei jüngeren Patienten für eine MRT ist der Verdacht auf eine chronisch-entzündliche ZNS-Erkrankung, eine Multiple Sklerose (MS) oder auch Encephalomyelitis disseminata (ED), Tab. 15.5. Diese ist durch Entmarkungsherde in der weißen Substanz gekennzeichnet. Bei ausgeprägten Erkrankungen sind die Veränderungen als hahnenkammartiges Muster in der sagittalen Flair entlang des Balkens zu erkennen. Die Erkrankung kann auch das Myelon betreffen. Hier sind die Veränderungen überwiegend in axialen Bildern dorsolateral lokalisiert. Findet man Veränderungen in der Nativ-Untersuchung, stellt sich immer die Frage, ob es sich um aktiv-entzündliche Veränderungen handelt. Hierzu werden T1-gewichtete Sequenzen in aller Regel in 2 Ebenen nach Kontrastmittelgabe angefertigt.
Tab. 15.5
Untersuchungsprotokoll Wirbelsäule bei MS/ED
Patientenvorbereitung | Sämtliches Metall, Scheckkarten, Schmuck etc. ablegen lassen |
Positionierung | Rückenlage, evtl. Knie unterpolstern |
Spule | Wirbelsäulenspule und Halsspule |
Scanbereich | HWS, BWS und obere LWS mit Conus caudae |
Kontrastmittel | Bei pathologischem Befund |
Sequenzen | Sagittale T1w, sagittale T2w, axiale T2w, axiale T1w; Nach Kontrastmittelgabe: sagittale und axiale T1w |
Kortison schließt innerhalb von 48 Stunden die Blut-Hirn-Schranke, durch die das Kontrastmittel treten muss. Eine Kontrastmittelgabe später als 48 Stunden nach Beginn einer Kortisontherapie macht daher keinen Sinn.
Sollten Sie im Myelon eine Syrinx, also eine flüssigkeitsisointense, zumeist längliche Läsion nachweisen können, muss in aller Regel bei der Erstdiagnose eine Kontrastmittelgabe erfolgen, um einen hierfür ursächlichen Tumor wie ein Ependymom auszuschließen.
15.3 Nuklearmedizinische Diagnostik
U. Blum8
(8)
Praxis für Nuklearmedizin, Strassburger Allee 2-4, 45481 Mülheim, Deutschland
15.3.1 Gehirn
Durchblutung, regionaler zerebraler Blutfluss (rCBF)
Der regionale zerebrale Blutfluss (rCBF, Tab. 15.6) kann mittels verschiedener Tracer dargestellt werden. Die Fragestellungen reichen von Fokusdarstellungen bei der Epilepsie über psychiatrische Erkrankungen, einer Aussage über die Perfusionsreserve des Gehirns bei vorangegangenen TIA’s bis hin zur Hirntoddiagnostik.
Tab. 15.6
rCBF-Untersuchung SPECT
Patientenvorbereitung | Anamnese. Blasenentleerung. Venenverweilkatheter legen und fixieren. Patient 30 min in einem abgedunkelten, ruhigen Raum ruhen lassen (ggf. Diamox nach 15 min). Injektion des Radiopharmakon über den Verweilkatheter. Patient erneut 15 min ruhen lassen. Sedierung (falls notwendig) erst nach der Injektion des Radiopharmakons |
Aktivität | 550 MBq 99mTc-ECD oder -HMPAO, min. 110 MBq |
Applikation | Nach Ruhephase i. v. |
Akquisition | Aufnahmebeginn 40 min p. i. (bis maximal 3,5 h p. i.) Rückenlage, Kopf fixiert SPECT (A. e. 3-Kopf-Kamera) LEHR (-FAN), Kollimator möglichst eng einstellen 128 * 128 Matrix, Projektionen je nach Kamerasystem Gesamtzählrate > 5 Millionen cts |
Auswertung | SPECT-Rekonstruktion als gefilterte Rückprojektion Darstellung der Bilder Ggf. 3D-Quantifizierung, ROI-Analysen |
Strahlenbelastung | ECD: 0.011 mSv/MBq → 6 mSv HMPAO: 0,0093 mSv/MBq → 5 mSv Bei Kindern ist die Strahlenbelastung/MBq höher: ECD 0,023 mSv/MBq, HMPAO 0,026 mSv/MBq |
Bei verschiedenen Fragestellungen sind verschiedene Hirnareale von besonderem Interesse, z. B. die Suche nach einem Fokus bei epileptischen Anfällen oder die Identifizierung des Sprach- oder Sehzentrums vor einer geplanten Operation.
Es stehen 99mTc-ECD (Ethylcysteinat-Dimer) und 99mTc-HMPAO (Hexamethylpropenylenaminooxim) zur Verfügung. Beide Substanzen sind fast gleichwertig.
Bei Fragen nach überlebendem Hirngewebe nach einem Hirninfarkt wird ECD eingesetzt, da es sich in den noch durchbluteten, jedoch abgestorbenen Gehirnzellen nicht anreichert. Eine weitere Domäne des ECD ist die Entzündungsdiagnostik. Zudem ist der Kontrast zwischen grauer und weißer Hirnsubstanz insbesondere im Temporallappen besser als bei HMPAO.
Andere Möglichkeiten der Bestimmung und Darstellung des rCBF liegen in der PET (Tab. 15.7).
Tab. 15.7
rCBF-Untersuchung PET
Patientenvorbereitung | Nüchtern Anamnese, wichtig: nach Diabetes fragen Venenverweilkatheter legen und fixieren Patient vor der Injektion ruhen lassen (Dunkler, ruhiger Raum) Blutzucker messen (< 120 mg/dl) Injektion des Radiopharmakon über den Verweilkatheter Patient ruhen lassen (länger als bei ECD/HMPAO) |
Aktivität | 300- 600 MBq 18F-FDG Kinder 5-10 MBq/kg; min. 10 MBq |
Applikation | In der Ruhephase i. v. |
Akquisition | Aufnahmebeginn 30–60 min p. i. Rückenlage, Kopf fixiert Schwächungskorrektur |
Auswertung | Gefilterte Rekonstruktion Darstellung der Bilder Ggf. ROI-Quantifizierung |
Strahlenbelastung | Erwachsene: 0.027 mSv/MBq Kinder: 0,073 mSv/MBq |
Hierbei können 15O markiertes Wasser (H2 15O) oder 15O-Butanol eingesetzt werden. Diese Produkte haben jedoch mit 2 Min eine sehr kurze Halbwertzeit, sodass ein Zyklotron in unmittelbarer Nähe verfügbar sein muss.
Da die rCBF mit dem regionalen Zuckerstoffwechsel verbunden ist, kann auch 18F-FDG eingesetzt werden.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree