und Christine Nowarra2
(1)
Bremener Str. 40, 46145 Oberhausen, Deutschland
(2)
Klinik für Radiologie Neuroradiologie, Klinikum Dortmund gGmbH, Beurhausstr. 40, 44137 Dortmund, Deutschland
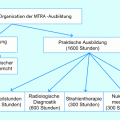
Sabine ist im 2. Semester der MTRA-Ausbildung und steht kurz vor ihrem ersten Einsatz am CT.
„Das wird sicher total spannend“, berichtet sie am Abend aufgeregt ihrem Freund Thomas. „Und noch in einer Unfallklinik. Da seh` ich sicher jede Menge. In der Schule lernen wir zwar noch sehr viele konventionelle Röntgenaufnahmen, aber in der Praxis wird doch mehr und mehr am CT gemacht. Heutzutage geht z. B. die Diagnostik eines Polytraumas im CT viel schneller und besser. Überhaupt möchte ich lieber im Bereich der Großgeräte und in der Schnittbilddiagnostik arbeiten. Das klingt doch schon spannender, findest du nicht?“ redet sich Sabine richtig in Rage. Thomas versucht aufmerksam zuzuhören, obwohl er nur Bahnhof versteht. „Nur das mit der Strahlenbelastung finde ich nicht so gut“, erzählt Sabine unbeirrt weiter. „Aber da habe ich vor kurzem einen Artikel über ‚Low-Dose-CT‘ gelesen. Ist schon toll, wenn man das alles richtig gut kann. Aber ich habe noch immer nicht den Unterschied zwischen Single- und Multi-Slice verstanden.“
„Du weißt schon, dass ich aus einer anderen Branche komme und kein Wort verstanden habe, oder?“ fragt Thomas und nimmt sie in die Arme.
?
1. Was ist der Unterschied zwischen sequentiellen CT-Untersuchungen und Spiral-CT-Untersuchungen?
2.
Mit welchem Wert wird die Strahlenabsorption im CT-Bild gemessen?
3.
Was ist der Pich?
5.1 Aufbau und Funktionsweise eines Computertomographen
K. Kara3
(3)
Bremener Str. 40, 46145 Oberhausen, Deutschland
5.1.1 Allgemeines und Möglichkeiten
Die Computertomographie (CT) ist ein Verfahren zur Erzeugung von Schnittbildern mittels Röntgenstrahlen. Aufgrund der rasanten Untersuchungszeit der modernen Geräte ist sie bei der Notfalldiagnostik die Methode der Wahl. Dabei wird das aufzunehmende Objekt der Strahlung ausgesetzt und die Schwächung bestimmt. In diesem Strahlengang befindet sich unterschiedliches Gewebe mit unterschiedlicher Dichte. Diese Dichtenunterschiede werden gemessen und in transversalen Körperschichten dargestellt.
Anders als bei den konventionellen Röntgenbildern (CR) entsteht hier eine überlagerungsfreie Darstellung unterschiedlicher Strukturen sowie eine räumliche Abgrenzung dieser in jeglicher Ebene. Demnach sind CT-Bilder Substitutionsbilder und konventionelle Bilder Summationsbilder. Somit können die genaue Zuordnung und das Ausmaß einzelner Organe und Pathologien bestimmt werden.
Jede aufgenommene Schicht besteht aus Voxeln und ist eine 2D-Darstellung. Ein Voxel setzt sich zusammen aus:
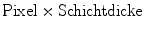
Dadurch bestehen einige Möglichkeiten der Nachbearbeitung der aufgenommenen Datensätze, wie die 3D-Dastellung, worauf später noch eingegangen wird (s. Postprocessing).
5.1.2 Geschichte
Der erste Computertomograph wurde in den 1970er Jahren von Sir Godfrey Hounsfield entwickelt, der für diese Entwicklung 1979 den Nobelpreis erhielt.
Finanziell unterstützt wurde Hounsfields von der Plattenfirma EMI, die die Beatles unter Vertrag hatte. Der erste Scanner wurde aus diesem Grund auch EMI-Scanner genannt, womit Schädel-CT’s durchgeführt wurden.
Da die Computer damals noch nicht so gut entwickelt waren, war die Auflösung gering (80 × 80) und die Untersuchungszeit sehr lang (ca. 10 min/Bild). Jedoch war dies die erste Möglichkeit, große Hirnprozesse zu diagnostizieren, ohne den Patienten „zu öffnen“. Daher wurden die ersten Schädeluntersuchungen zum Ausschluss eines Tumors oder einer Blutung durchgeführt sowie zur Beurteilung der Ventrikelweite.
Heute werden zu Ehren von Hounsfield die Einheiten der Schwächungswerte in Hounsfield Units (HU) bzw. Hounsfieldeinheiten (HE) angegeben.
5.1.3 Aufbau
Der Computertomograph besteht aus vielen einzelnen Elementen, die jedoch alle zusammen fehlerfrei funktionieren müssen, um eine patientengerechte und hochqualitative Untersuchung durchführen zu können. Im Folgenden wird auf die wichtigsten Einzelteile eingegangen.
Gantry
Die Gantry ist das, was man außer dem Tisch sieht, wenn der Untersuchungsraum betreten wird (Abb. 5.1). Sie wird als das „Herz“ des Tomographen bezeichnet, denn unter der Abdeckung befinden sich Röntgenröhre, Blendensystem, Detektorsystem, Kühlsystem sowie mechanische Elemente. Die gesamte Gantry kann (je nach Gerätetyp) horizontal bis zu +/- 30° gekippt werden.

Abb. 5.1
Gantry. Zu diesem Bild ist ein Video online verfügbar auf www.springermedizin.de/vzb-Hartmann. (Mit freundlicher Genehmigung von Mario Voss, Siemens)
Bei einer CT rotieren die Röhren-Detektorsysteme mit einem Gewicht von 2–3 t (Dual-Sorce-Systeme sogar 4–5 t) um den Patienten. Durch die schnelle Röhrenrotation (bis zu < 0,3 s/Rotation) entstehen hier immense Fliehkräfte.
Röntgenstrahler
Das Prinzip des Röntgenstrahler s wurde bereits im Kapitel 3 erläutert. Auch hier ist es ein Vakuumgefäß mit einer Anode und Kathode zur Erzeugung von Röntgenstrahlen. Für den CT wurde jedoch ein neuer Strahler konzipiert und gebaut. Es handelt sich hier um einen sog. Drehgehäusestrahler. Hier rotiert nicht nur die Anode, sondern das gesamte Gehäuse, und somit auch die Kathode. Dadurch, dass die Anode die Außenwand des Gehäuses bildet, findet eine direkte Kühlung statt. Demnach verlängert und verbessert sich die Fähigkeit der Röhrenleistung. Die Kühlflüssigkeit ist Öl (Abb. 5.2). Eine weitere Besonderheit bei diesen Strahlern ist die elektromagnetische Fokussierung des Elektronenstrahls, d. h. der Elektronenstrahl wird auf dem Weg von der Kathode zur Anode ständig so abgelenkt, dass auf der Anode ein gewünschter Brennfleck bzw. eine gewünschte Brennfleckgröße entstehen. Diese Methode der Ablenkung wird auch genutzt, um zwei Brennflecke zu erzeugen (siehe hierzu z-sharping/Springfokus).
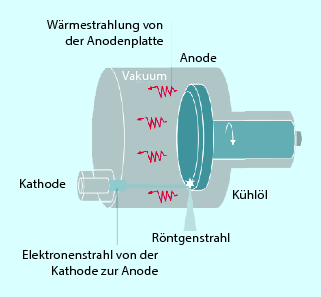
Abb. 5.2
Aufbau eines CT-Röntgenstrahlers. (Mit freundlicher Genehmigung der Siemens AG, Healthcare Sector)
Generator
Die wichtigste Aufgabe des Generators ist es, kontinuierlich die gewünschte Leistung zu gewähren. Es müssen Spannungen von 80–140 kV erzeugt werden. Auch die Röhrenstromerzeugung (mA) muss stabil und schnell erfolgen. Die zeitliche Komponente spielt bei beiden Parametern eine wichtige Rolle, denn die Untersuchungen laufen heute sehr schnell ab. So muss während einer schnellen Untersuchung umso schneller die Dosismodulation erfolgen. Dosismodulation bedeutet die Anpassung von kV und mA an das durchstrahlte Objekt. Beispielsweise benötigt man bei einem CT-Abdomen für den Oberbauch weniger Dosis als für die Beckenpartie, sodass hier eine Hochregulierung der Parameter erforderlich ist. Somit wird erstens die geringere Dosis für den Oberbauch eingehalten, und zweitens wird die Bildqualität im Gesamten gewährleistet. Dazu später mehr.
Blendensysteme
Die Blendensysteme bestehen aus Blei und unterscheiden sich in ihrer Form und Funktion.
Am Fokus befinden sich Blenden zur Einstellung des Fächerstrahls. Dies erlaubt die Kontrolle der auf den Patienten fallenden Dosis. Feste Blenden sorgen für das Nichtüberschreiten der maximal erlaubten Fächerbreite. Hinter dem Patienten, vor dem Detektorsystem, sind flexible Blenden vorhanden. Diese dienen der Schichtdickeregulierung. Die Streustrahlenabsorption erfolgt durch kleine Bleilamellen zwischen den Detektorelementen. Ähnliches haben Sie bereits im Kapitel „Konventionelle Röntgendiagnostik (Kap. 3)“ als Streustrahlenraster kennengelernt.
Patiententisch
Der Patienten- oder Untersuchungstisch dient der optimalen Positionierung des Patienten. Er kann sowohl in der Höhe als auch in der Längenausrichtung verändert werden. Wichtig sind die exakte Positionierungsmöglichkeit und der stabile Tischvorschub während einer Untersuchung. Die modernen Scanner können mit einem geeigneten Tisch eine Strecke von bis zu 2 m untersuchen. Auch können diese je nach Modell bis zu ca. 240 kg belastet werden.
Bildrechner
Die technische Steuerung erfolgt durch den Bildrechner. Nachdem die Akquirierung auf gewünschte Weise erfolgt, verändert diese Rechnereinheit die Rohdaten mittels Algorithmen – ebenfalls in gewünschter Form. Die Rohdaten werden bearbeitet und umgerechnet, sprich rekonstruiert. Auf die Rekonstruktionsalgorithmen wird in Abschn. 5.1 explizit eingegangen. Auch dient der Bildrechner als kurzer Zwischenspeicher zur späteren Rekonstruktionsmöglichkeit.
Konsole/Workstation
Diese Einheit dient der Durchführung der Untersuchung. Nach der Patientenlagerung und -einstellung kann die gewünschte Region bzw. das gewünschte Organ mit den entsprechenden Parametern akquiriert werden. Es gibt nur eine Haupt-Workstation. Manche Abteilungen haben zur weiteren Bearbeitungen bzw. Rekonstruktionen ein angeschlossenes zweites Monitorsystem.
Detektorsystem/-typen
Die primäre Aufgabe eines Detektors besteht darin, die durch ein Objekt geschwächte Röntgenstrahlung zu registrieren bzw. zu messen (also die Strahlung, die durch den Patienten durchgedrungen ist), und muss sich demnach hinter dem durchstrahlten Objekt befinden. Diese Strahlen werden in elektrische Signale umgewandelt. Hinter dem Detektorsystem befinden sich das DAS (= Daten-Akquisitions-Systeme) zur Erfassung dieser Signale und Weiterleitung an den Rechner, wo die Erzeugung bzw. Rekonstruktion der digitalen Bilder stattfindet.
Im Folgenden werden der Aufbau und die Funktion bestimmter Detektorsysteme vorgestellt. Auch hier kam es im Laufe der Zeit zu Veränderungen. Zu Beginn bestanden die Detektoren aus Hochdruck-Ionisationskammern, die mit Xenon gefüllt waren. Xenon ist ein Edelgas, weshalb diese Detektoren Gasdetektoren genannt wurden. Xenongas wurde durch die Röntgenstrahlen ionisiert (Abb. 5.3). Die Elektronen-Ionenpaare wanderten zu den Hochspannungs- und Messelektroden. Elektronen wanderten zu den Hochspannungselektroden und Ionen zu den Messelektroden. Diese Elektroden waren auf dem Detektor abwechselnd gereiht und besaßen eigene Messkanäle, wodurch die Datenaufnahme parallel erfolgte. Die Zwischenräume bildeten die eigentlichen Detektorelemente. Der gemessene Signalstrom wurde zur Bildentstehung dem Rechner zugeführt. Jedoch brachte dieses Detektormodell auch mehrere Probleme mit sich. Das größte Problem lag in der geringen Quanteneffizienz. Nur 50 % der einfallenden Röntgenstrahlung konnte im Detektor erfasst werden. Somit dienten wenige Signale der Bildentstehung. Dies hatte zur Folge, dass der Patient einer höheren Strahlenexposition unterlag. Ein weiteres Problem entstand, als die Mehrzeilen-CT entwickelt wurde, denn das Bauen mehrzeiliger Gasdetektoren war technisch nicht möglich.
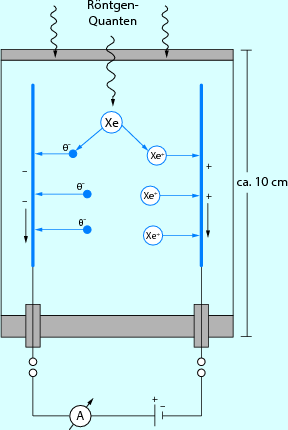
Abb. 5.3
Grundaufbau von Detektorsystem en
Die Detektoren der Computertomographen der Mehrzeilengeneration sind Festkörperdetektoren mit Szintillationskristallen (Abb. 5.4). Der Festkörperdetektor bzw. die -elemente bestehen aus keramischem oder kristallinem Material (z. B. Cadmium-Wolframat oder Cäsium-Iodid), das auf einer Photodiode sitzt. Zwischen den einzelnen Detektorelementen befinden sich zur Abtrennung Wolfram- oder Molybdänbleche.
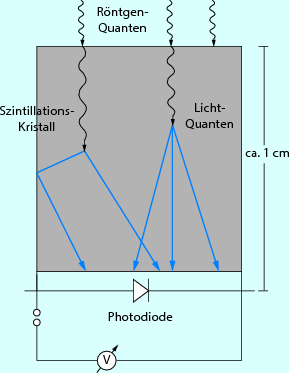
Abb. 5.4
CT-Festkörperdetektor mit Szintillationskristallen
Sobald Röntgenstrahlung auf den Kristall fällt, kommt es zu einer Ionisation. Es entstehen Lichtblitze. Die Photodiode nimmt diese auf und wandelt sie in elektrische Signale um. Nach der Signalverstärkung kommt es durch die DAS zur Signalweiterleitung an das Rechnersystem, wo die Bilderzeugung stattfindet.
Wahl und Vorteil der Keramikdetektoren sind die hohe Quanteneffizienz, also die hohe Absorption der einfallenden Röntgenstrahlen. Somit entstehen viele Lichtblitze, die der Bildentstehung dienen. Weitere wichtige Aspekte sind die schnelle Abklingzeit des Signals und das geringe Nachleuten des Kristalls nach der Ionisation. Diese Punkte sind für die moderne Gerätetechnologie und für die hohe Ortsauflösung essenziell, denn die Rotationszeiten sind sehr gering (ca. 0,3 s pro Umlauf) und die Anzahl der Projektionen, durch mehrzeilige Detektoren, sehr hoch.
Auf die zwei verschiedenen Detektortypen „Fixed Array Detektor“ und „Adaptive Array Detektor“ wird im Abschn. 5.1.5 „Multislice-CT“ eingegangen.
5.1.4 Gerätegeneration
Die bereits erwähnt, kam der erste CT in den 1970er Jahren auf den Markt. Die Aufnahme erfolgte im Translation-Rotations-Prinzip. Die Röntgenstrahlung wurde in einem Nadelstrahl ausgesandt, durchstrahlte das Objekt und traf auf den Detektor. Die Röntgenröhre und der Detektor wurden danach seitlich verschoben (→ Translation) und das Objekt wieder durchstrahlt. Danach erfolgte eine Rotation um einen bestimmten Winkel und die erneute Akquisition.
Das Prinzip der 1. Generation wurde in der nächsten, der 2. Generation, beibehalten (Abb. 5.5a, b). Der wesentliche Unterschied bestand darin, dass die Röntgenstrahlung in einem Teilfächerstrahl emittiert wurde und statt einem Detektor mehrere Detektoren eingesetzt wurden. Dies führte zu erster enormer Zeitreduktion von ca. 5 min/Schicht auf ca. 20 s/Schicht!
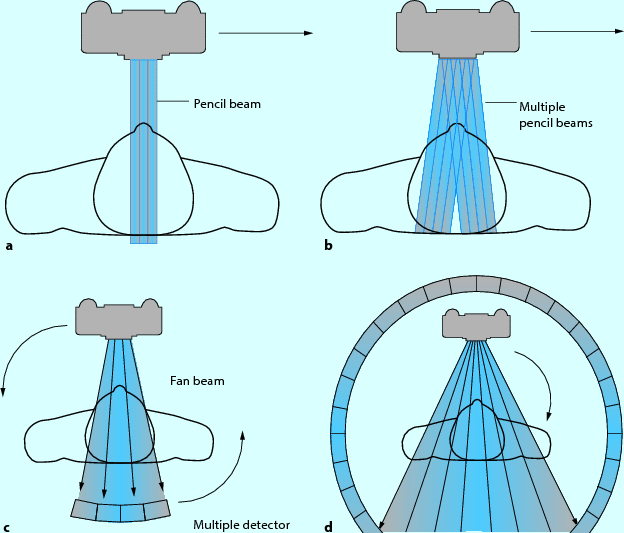
Abb. 5.5a–d
Gerätegenerationen . a Erste Generation; b zweite Generation; c dritte Generation; d vierte Generation
Die ersten beiden Generationen konnten lediglich für Schädeluntersuchungen eingesetzt werden.
Die Technik der 3. Generation ist die etablierte Technik, die heute angewandt wird (Abb. 5.5c). Diese Computertomographen werden auch Rotate-Rotate-Geräte genannt. Hier bewegen sich Röntgenröhre und Detektor simultan, also gleichzeitig um den Patienten. Die Röntgenstrahlung wird als Fächerstrahl emittiert. Jedoch verbirgt sich auch hier eine Besonderheit: der Fächerstrahl erfasst den gesamten Körperquerschnitt. Von nun an konnten weitere Organe untersucht werden.
Die Rotate-Stationary-Geräte wurden in der 4. Generation entwickelt (Abb. 5.5d). Neu war hier der 360°-Detektor in Form eines Ringes. Die Detektorelemente deckten die gesamte Gantry ab. Somit brauchte nur noch der Röntgenstrahler um den Patienten zu rotieren. Diese Technik konnte sich jedoch nicht etablieren. Die Kosten waren zu hoch, die Bildqualität nicht optimal. Sie wurde aufgegeben.
5.1.5 Untersuchungstechniken
Es gibt verschiedene Möglichkeiten, eine computertomographische Untersuchung durchzuführen. Dies hängt vom Gerätemodell und der Untersuchung bzw. der klinischen Fragestellung ab. Wichtig ist jedoch bei jeder Untersuchung die Lagerung! Das aufzunehmende Objekt muss isozentrisch gelagert werden, d. h. in der Mitte des Strahlengangs liegen oder besser: Durch die isozentrische Lagerung befindet sich das aufzunehmende Objekt während der Aufnahme und der Rotation immer im Zentrum des Strahlengangs. Das ist ein sehr wichtiger Punkt für die Dosisregelung, die Ortsauflösung und somit die Bildqualität.
Der eigentliche Beginn einer jeden Untersuchung ist die Aufnahme eines Übersichtsbildes, dem Topogramm, auch Scout oder Surview genannt. Auf dieser Übersicht erfolgt die Eingrenzung des zu untersuchenden Bereichs mittels eines „Rechtecks“, der Range oder Field-of-View (FOV). Dieser Bereich wird mit den bereits voreingestellten Parametern aufgenommen. Auf die Parameter wird separat eingegangen. Sehr wichtig ist sich vor Augen zu halten, dass die Range in der cranio-caudalen Ausrichtung die Enddosis mitbeeinflusst, denn:
Je länger/größer die Range und somit die Scanstrecke, desto länger die Bestrahlungsdauer und höher die Strahlenbelastung!
Sequenz-CT
Die Technik der sequenziellen Aufnahme ist die erstentwickelte Technik. Die wird auch „Step and Shoot“ genannt. Es werden Schicht für Schicht transversale/axiale Aufnahmen durchgeführt. Zwischen zwei Aufnahmen ist eine Tischbewegung nötig – axiale Schicht → Tischbewegung → axiale Schicht → „Step and Shoot“. Vorteil ist hier die Möglichkeit der direkten Bildanschauung des Untersuchers und Befunders, da die zu rekonstruierende Datenmenge gering ist und sofort erfolgen kann. Ein großer Nachteil ist jedoch die lange Untersuchungszeit. Auch besteht das Risiko der Nichterfassung kleinster Details zwischen zwei Schichten durch eine nichtkontinuierliche Datenerfassung (Abb. 5.6). Dadurch besteht keine Möglichkeit der dreidimensionalen Darstellung.
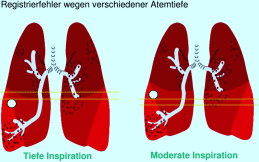
Abb. 5.6
Nichtkontinuierliche Datenerfassung aufgrund unterschiedlicher Atemtiefe. (Mit freundlicher Genehmigung der Siemens AG, Healthcare Sector)
Haupteinsatzgebiet ist mittlerweile die Intervention und prospektiv getriggerte Kardio-CT s. Teilweise werden Schädel-CT s heute noch sequentiell akquiriert, um mit gekippter Gantry die Augenlinsen als sehr strahlensensible Strukturen nicht dem Direktstrahl auszusetzen. Durch moderne Gerätetechniken wird diese Technik jedoch zunehmend durch die der Spiralaufnahmen ersetzt.
Dynamische CT
Dynamische CT-Aufnahmen erfolgen hauptsächlich auch in sequenzieller Technik. Der Unterschied besteht darin, dass nur eine ausgewählte Schichtposition kontinuierlich aufgenommen wird. Dadurch ist es möglich, beispielsweise Flussmessungen durchzuführen und somit physiologische Vorgänge zu repräsentieren und zu beurteilen. Diese Messungen können nur mithilfe von Kontrastmitteln erfolgen. Durch das Kontrastmittel wird der Blutfluss dargestellt, sodass die Kinetik erfasst und gemessen wird. Es können unter anderem Aussagen über Organperfusionen oder auch über die Herzauswurfrate („Cardiac output“) getroffen werden. Eine sehr große und essentielle Rolle spielt die dynamische CT-Untersuchung bei der „Stroke Unit“, also für akute Schlaganfallpatienten im Zeitfenster von 4,5 h nach Erstsymptomatik. Hier ist die sehr schnelle interdisziplinäre Zusammenarbeit lebenswichtig, denn „TIME IS BRAIN“! Mittels der Computertomographie und der Perfusionsmessung des Gehirns kann das nichtdurchblutete Hirnareal detektiert und das dazugehörige Stromgebiet bzw. die Arterie, die dieses Areal versorgen sollte, mittels spezieller Medikamente im Anschluss therapiert werden (Lysetherapie).
Die Bolustriggerung ist ebenfalls eine dynamische Aufnahmetechnik. Auf der gewählten Schichtposition wird kontinuierlich die Kontrastmittelanreicherung im fokussierten Gefäßlumen gemessen. Bei Erreichen der voreingestellten und vorbestimmten Dichte (HU) startet das Gerät automatisch und akquiriert die gewünschte Region.
Spiral-CT/Singleslice-CT (SS-CT)
Mit der Einführung der Spiral-CT s in den frühen 1990er Jahren kamen neue Möglichkeiten in den Klinikalltag. Die Datenerfassung erfolgte nicht mehr „nur“ sequenziell, sondern auch spiralförmig, helixartig oder helikal genannt. Mit kontinuierlichem Tischvorschub und kontinuierlicher Röhrenrotation wird das aufzunehmende Objekt im gesamten Volumen erfasst, und es entstehen keine Datenlücken. Zur Erfassung der Daten ist eine Detektorreihe vorhanden → Singleslice (Abb. 5.7). Dank der Spiralakquisition erfolgt die Abdeckung der Untersuchungsregion sehr schnell. Dadurch verkürzen sich die Untersuchungszeiten so stark, dass innerhalb einer Atemphase die Untersuchung durchgeführt werden kann. Automatisch kann die Kontrastmittelmenge ebenfalls reduziert werden. Aufgrund der lückenlosen Volumenabdeckung bestehen nun die Möglichkeiten der überlappenden Rekonstruktion – die multiplanaren Reformation (2D) und die 3D-Darstellung.
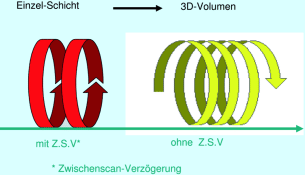
Abb. 5.7
Singleslice-CT. (Mit freundlicher Genehmigung der Siemens AG, Healthcare Sector)
Multislice-CT (MS-CT)
1998 kam der erste MS-CT auf den Markt, ein „4-Zeiler“. Hier sind vier Detektorreihen vorhanden. Dies bedeutet, dass bei einer Röhrenrotation um den Patienten direkt vier Schichten erfasst werden, also eine größere Volumenabdeckung stattfindet (Abb. 5.8). Somit bekommt man eine schnellere Volumenerfassung und dadurch kürzerer Untersuchungszeiten, folgend auch wieder eine KM-Reduktion. Einen weiteren Vorteil bringen die Multislices in der Nachverarbeitung. Durch die Aneinanderreihung mehrerer Detektoren gelingt eine isotrope Voxelgeometrie, was wichtig für die 3D-Darstellung ist. Isotrop bedeutet, dass alle Kantenlängen gleich groß sind. Dadurch ist eine gute Ortsauflösung gegeben.

Abb. 5.8
Multislice-CT . (Mit freundlicher Genehmigung Siemens AG, Healthcare Sector)
Die Detektoren der MS-CT unterscheiden sich in ihrer Form und ihrem Typ. Es gibt zwei Detektorarten, „Fixed Array Detektor“ und „Adaptive Array Detektor“.
Fixed Array Detektor (Abb. 5.9): Feste Größen der Detektorelemente pro Detektorzeile. Durch die Anwahl bestimmter Detektorzeilen kann die Schichtdicke bestimmt werden.
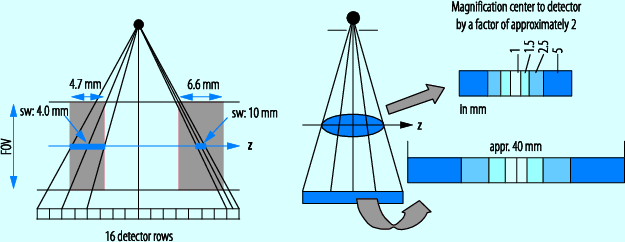
Abb. 5.9
Fixed und Adaptive Array Detektor. (Aus Lecoq 2011)
Adaptive Array Detektor (Abb. 5.9): Die Größen der einzelnen Detektorelemente nehmen von innen nach außen zu. Dies führt zu der Möglichkeit, einzelnen Elemente und Zeilen miteinander zusammenzuschalten. Somit besteht die Option unterschiedlicher Schichtdicken. Durch den matrixartigen Aufbau der Detektorelemente wird dieser Detektor auch „Matrix-Detektor“ genannt.
Wichtige Parameter und Zusammenhänge im Spiral-CT
Wie bereits beschrieben bewegen sich bei Spiral-CTs der Patiententisch und der Scanner kontinuierlich. Durch den gleichmäßigen Tischvorschub erfolgt eine spiralförmige Datenaufnahme mit den o. g. Vorteilen. Jedoch spielen hier viele Parameter und Elemente eine wichtige Rolle:
Parameter zur Datenakquisition
Pitchfaktor (p)
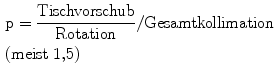
Der Pitchfaktor bestimmt, ob eine Datenakquisition überlappend (p < 1), lückenlos (p = 1) oder mit Datenaussparung, sog. Gap, (p > 1) erfolgt und reguliert die Schnelligkeit des Tischvorschubs und somit auch die Untersuchungsdauer. Die Dosis wird zwar sekundär, aber ebenfalls beeinflusst. Bei einer überlappenden Volumenerfassung werden mehr Daten erfasst als bei einer Volumenerfassung mit kleinen Lücken. Somit wird für überlappende Aufnahmen mehr Strahlung angewendet als für die mit „Gaps“.
Röhrenspannung (kV)
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree