und Kai Reiter2
(1)
Klinik für Radiologie Neuroradiologie, Klinikum Dortmund gGmbH, Beurhausstr. 40, 44137 Dortmund, Deutschland
(2)
Amundsenweg 35, 45472 Mülheim an der Ruhr, Deutschland
Nicole ist 36 Jahre alt und seit 17 Jahren als MTRA tätig. Vor ein paar Monaten konnte sie endlich ihren Wunsch durchsetzen am MRT eingearbeitet zu werden. Dieses Gerät war bislang nur den „Cracks“ vorbehalten und es hat ewig gedauert, bis einige andere Kollegen, die vor ihr „dran“ waren, endlich eingewiesen waren. Aber inzwischen werden selbst die MTRA-Schüler während der praktischen Ausbildung dort eingearbeitet! Da kann man, Nicoles Meinung nach, als erfahrene MTRA ganz schön dumm aussehen, wenn die Schüler so viel mehr wissen als man selbst.
Als Nicole die Ausbildung gemacht hat galt ein MRT noch als Exot und wurde im Unterricht kaum behandelt. „Ein Gerät, welches nicht strahlt und sehr kompliziert mit Radiowellen funktioniert“ war die zentrale Aussage ihres Unterrichtes. Und in der Klinik, in der sie die praktische Ausbildung absolvierte, gab es damals gar kein MRT. Wie sich die Zeiten geändert haben…
Inzwischen ist Nicole seit sechs Wochen im Frühdienst am MRT eingeteilt und hat schon viel gelernt. Die Standarduntersuchungen wie Schädel, Wirbelsäule oder Knie kann sie allein durchführen. Ihr Ziel ist es aber, mehr zu erfahren und an den Parametern „rumzuschrauben“ wie ihr Kollege. Der weiß genau was er wann machen darf, um z. B. eine Untersuchungszeit zu halbieren, ohne dass die diagnostische Aussagekraft der Untersuchung leidet. Sogar der Oberarzt hört manchmal auf ihn, wenn es um die Auswahl der richtigen Messsequenz für eine bestimmte Fragestellung geht.
Das möchte Nicole auch irgendwann beherrschen.
Jetzt muss aber erst mal Herr Schilling untersucht werden, der mit der Frage nach einem Meniskusschaden zur Knie-MRT gekommen ist.
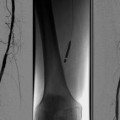
Herr Schilling, ein 46-jähriger Patient kommt in die Radiologie für eine Kernspinuntersuchung des linken Kniegelenks. Der Patient gibt an, beim Joggen ein „Knacken“ im Knie verspürt zu haben und hat seitdem Schmerzen im Kniegelenk beim Beugen. Beim Steinmann-Test des Orthopäden hat sich der Verdacht eines Meniskusschadens ergeben. Das Röntgen des Kniegelenkes zuvor in zwei Ebenen war unauffällig (Abb. 6.1).
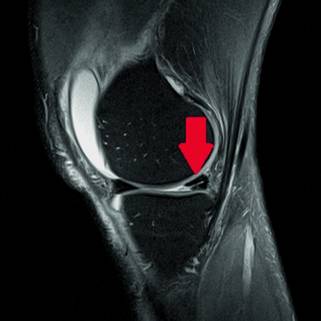
Abb. 6.1
Sagittales protonendichtes Bild vom Knie mit Fettsättigung. In der Schicht zeigt sich eine komplexe Innenmeniskushinterhornruptur (roter Pfeil) mit begleitendem Kniegelenkserguss
Stellen Sie sich vor, dass Sie in Ihrer Ausbildung zur MTRA gerade beim Bereich „Kernspintomographie“ angekommen sind:
1.
Welche Spule benötigt man für die Kernspintomographie des Kniegelenks?
2.
Der MTRA hat Ihnen kurz telefonisch mitgeteilt, dass er etwas später zur Untersuchung kommt und bittet Sie, den Patienten schon mal vorzubereiten. Was müssen Sie beachten?
3.
Wann darf ein Patient nicht im Kernspintomographen untersucht werden?
6.1 Physikalische Grundlagen der Kernspintomographie
6.1.1 Magnetresonanztomographie = Kernspintomographie
Die Kernspintomographie wird auch als Magnetresonanztomographie (MRT) bezeichnet. Dabei werden mittels eines sehr starken statischen Magnetfeldes (B0), niederfrequenter Gradientenfelder (B1) und hochfrequenter elektromagnetischer Felder Protonen angeregt und mit Hilfe von Empfangsspulen die Signale aus dem Körper aufgefangen. Aus den Signalen wird mit einem Hochleistungscomputer ein anatomisches Bild berechnet.
Die MRT kommt ohne ionisierende Strahlung aus. Außerdem kann man hier die Schichtung nach dem Verlauf der zu untersuchenden Struktur anpassen. Ein weiterer Vorteil ist der hohe Weichteilkontrast, der mithilfe verschiedener Untersuchungsparameter exakt für die jeweilige Untersuchungsregion eingestellt werden kann.
6.1.2 Atommodell
Der menschliche Körper besteht zu zwei Drittel aus Wasser. Für die Kernspintomographie sind die Wasserstoffatome im menschlichen Körper von größter Bedeutung. Ein Wasserstoffatom besteht aus einem Kern und einer Hülle (Abb. 6.2). Auf der Atomhülle des Wasserstoffatoms ist ein Elektron mit einer negativen Ladung, und im Wasserstoffatomkern ist ein Proton mit einer positiven Ladung. Das Wasserstoffatom ist somit elektrisch neutral.
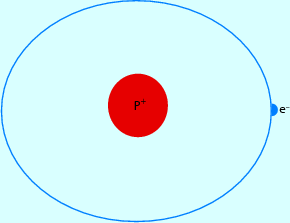
Abb. 6.2
Wasserstoffatom mit rotem Proton und blauen Elektron auf der Schale
Für die Kernspintomographie ist das Proton im Wasserstoffatom von größter Wichtigkeit, und wir werden uns im folgendem nur noch hiermit beschäftigen.
Das Proton rotiert zum einen um seine eigene Achse, wie ein Kreisel (Abb. 6.3). Dabei ist es bestrebt, seine Lage und Drehrichtung beizubehalten. Zum anderen fließt durch die Rotation der elektrischen Ladung ein Strom, der ein magnetisches Moment induziert. Somit kann das sich rotierende Proton auch als kleiner Stabmagnet betrachtet werden.
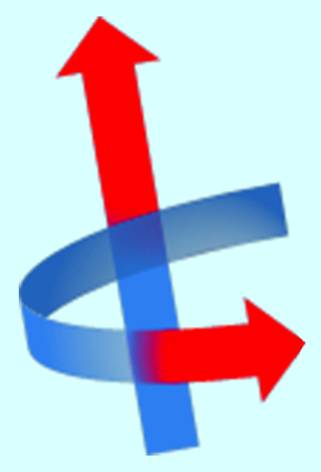
Abb. 6.3
Proton mit Spin um die eigene Achse
Unter normalen Bedingungen rotieren die Protonen im Körper rein zufällig in einer Richtung. Die Eigenschaft des Rotierens nennt man Spin , womit wir schon zwei Begriffe der Kernspintomographie erklärt hätten:
1.
das Proton im Wasserstoffkern,
2.
das Rotieren bzw. der Spin des Protons.
6.1.3 Wasserstoffprotonen im MRT
Setzt man die Spins einem starken Magnetfeld aus, so fangen diese an, entlang des äußeren Magnetfeldes zu präzedieren (taumeln, Abb. 6.4). Die Präzessionsbewegung ist abhängig von der äußeren Magnetfeldstärke, will heißen: Wie schnell die Protonen taumeln, hängt von der Stärke des Magneten ab und kann mit der Lamorbeziehung berechnet werden:
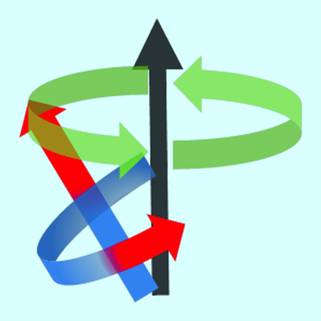
Abb. 6.4
Präzesionsbewegung des rein zufällig gewählten Spins im Magnetfeld
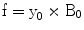
f bezeichnet die Lamorfrequenz in Megahertz (MHz).
γ0 bezeichnet das gyromagnetische Verhältnis und ist für ein Proton etwa 42,58 MHz/T.
B0 bezeichnet die Feldstärke in Tesla.
Somit liegt die Lamorfrequenz bei einer Feldstärke von 1 Tesla bei 42,58 MHz. Das bedeutet, dass bei 1 Tesla ein Proton 42.000.000 pro Sekunde taumelt.
Beim Auflegen des Patienten passiert aber noch was anderes mit den Protonen.
Es baut sich entlang des Magnetfeldes die sog. Längsmagnetisierung Mz auf. Hierbei handelt es sich um einen sehr komplexen Prozess. Dieser wird hier anhand eines Beispiels erklärt: Während sich etwa 1.000.000 Protonen antiparallel ausrichten, richten sich etwa 1.000.007 Protonen parallel aus (Abb. 6.5, Abb. 6.6). Der Grund hierfür liegt in der Tatsache, dass die antiparallele Ausrichtung mehr Energie benötigt. Der Überschuss von 7 Protonen, die sich parallel zum Magnetfeld ausgerichtet haben, trägt zur Bildgebung bei und entspricht der Längsmagnetisierung M Z . Dabei ist die Stärke des Magnetfelds entscheidend. Bedeutet also:
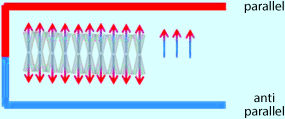
Abb. 6.5
Spin Ausrichtung im MRT mit einem geringen Überschuss parallel
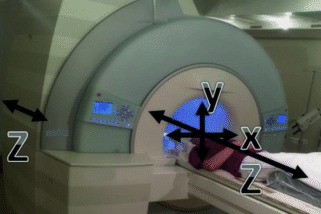
Abb. 6.6
Ausrichten der Spins entlang des statischen Magnetfelds in Z-Richtung. Nach der Anregung werden die Spins in die x-y-Ebene ausgelenkt
Je stärker das Magnetfeld, desto mehr Protonen richten sich parallel statt antiparallel aus und umso stärker ist die Längsmagnetisierung MZ.
6.1.4 Sequenz
Jetzt kann immer noch kein Signal im Körper unseres Patienten gemessen werden. Hierfür muss ein Hochfrequenzimpuls in Resonanz gleich der Lamorfrequenz geschaltet werden, sonst reagieren die Protonen nicht. Außerdem muss der HF-Impuls lang genug sein, um die Protonen aus der Längsmagnetisierung MZ in die transversalen Magnetisierung M XY umklappen zu lassen (Abb. 6.7). Wenn jetzt an der angeregten Stelle eine Empfangsspule aufliegt, kann hier ein „MR-Signal“ empfangen werden.
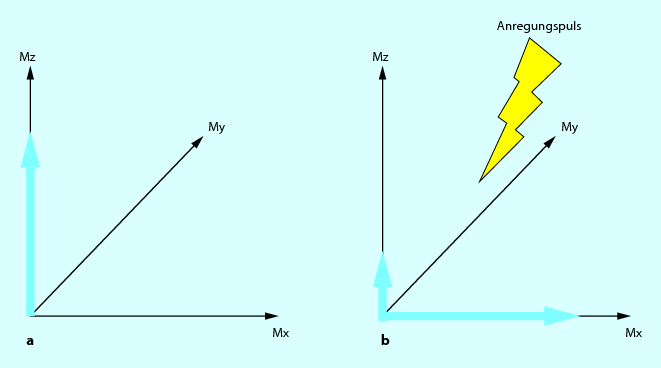
Abb. 6.7a,b
HF-Puls mit umgeklappten Magnetisierung
Wir haben jetzt im Schnelldurchlauf zwei für die Kernspintomographie wichtige Prozesse kennengelernt.
Longitudinalmagnetisierung
Transversalmagnetisierung
Diese beiden Prozesse laufen völlig unabhängige voneinander ab. Nach dem Einstrahlen eines HF-Impulses ist die Longitudinalmagnetisierung verschwunden, und die Protonen sind in der Transversalmagnetisierung.
6.1.5 Longitudinalrelaxation (T1-Relaxation)
Die Longitudinalmagnetisierung MZ baut sich nach dem Einstrahlen des HF-Pulses langsam wieder auf, während die Transversalmagnetisierung MXY abnimmt. Dabei geben die Protonen Energie an die Umgebung (dem sog. Gitter) ab, was sowohl als Spin-Gitter-Relaxation oder auch als T1-Relaxation bezeichnet wird. Wie schnell die T1-Relaxation abläuft, hängt vom jeweiligen Gewebe ab und wird durch die Magnetfeldstärke B0 beeinflusst (Abb. 6.8). Dabei verlängert sich die Zeit der T1-Relaxation mit zunehmender Feldstärke. Allerdings wird die T1-Relaxation nicht von Magnetfeldinhomogenitäten beeinflusst.
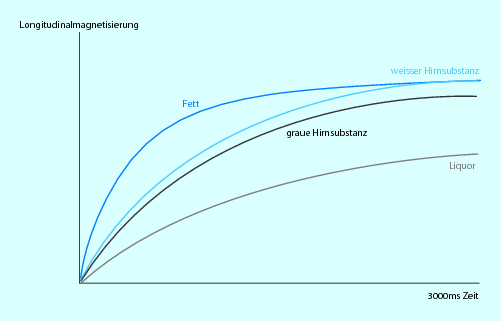
Abb. 6.8
T1-Relaxationkurve
6.1.6 Transversalrelaxation (T2-Relaxation)
Nach dem Einstrahlen des HF-Pulses sind die Protonen alle synchronisiert bzw. in sog. Phase (Abb. 6.9). Das Signal ist jetzt ganz stark. Jedoch dephasieren die Protonen ganz schnell wieder, weil die Protonen sich gegenseitig beeinflussen. Es werden kleine Magnetfelder erzeugt, die die Protonen unterschiedlich schnell präzedieren lassen. Dieser Vorgang wird auch als Spin-Spin-Relaxation bezeichnet und ist nicht vom äußeren Magnetfeld B0 abhängig.
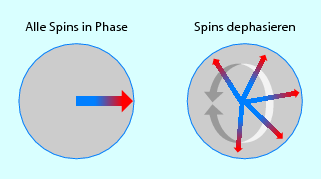
Abb. 6.9
Direkt nach dem HF-Puls sind die Spins alle in Phase. Jedoch dephasieren alle Spins sofort und sind zum Zeitpunkt „n“ an unterschiedlicher Stelle
6.1.7 Transversalrelaxation (T2*-Relaxation)
Ein weiterer Faktor, der sog. T2*-Zerfall , beeinflusst unsere Transversalrelaxation. Er ist abhängig von der Inhomogenität des äußeren Magnetfeldes B0 und von dem jeweils untersuchten Objekt. Dies hat zur Folge, dass die Signalintensität schneller abnimmt, als die eigentliche Transversalrelaxation erwarten lassen würde (Abb. 6.10). Es handelt sich um eine konstante Frequenz und lässt sich mit einem Refokussierungspuls teilweise rückgängig machen.

Abb. 6.10
T2-Relaxationskurve
Wichtige Charakteristika
Die Relaxationszeiten dienen als Mittel zur Kontrastierung, da T1- und T2-Relaxation gewebeabhängig sind.
Die T1-Relaxation dauert länger als T2-Relaxation.
Die T1-Relaxation ist abhängig von der jeweiligen Magnetfeldstärke.
6.1.8 Schichtselektion
In den letzten Abschnitten haben wir jetzt etwas von Präzession, Anregung und Relaxation erfahren. Bis jetzt empfangen wir nur ein Signal, welches bis jetzt aber keinerlei räumliche Zuordnung aufweist. Geht man davon aus, dass man ein homogenes Magnetfeld B0 hat, würde es im gesamten Körper ja dieselbe Präzessionsfrequenz zum Anregen bringen.
Man bedient sich eines Tricks. Es wird während des HF-Impulses ein zusätzlicher Schichtselektiongradient geschaltet, der dafür sorgt, dass das statische Magnetfeld sich minimal verändert und somit jede Schicht eine eigene Lamor- bzw. Präzessionsfrequenz besitzt.
Hierfür sind im Kernspintomographen drei zusätzliche Gradientenspulen eingebaut. Diese Gradientenspulen sind senkrecht zueinander in allen drei Raumebenen x-, y- und z-Richtung angelegt. Die einzelnen Gradientenspulen bestehen jeweils aus zwei Zylinder-Spulen, die beim Fließen eines Stromes auf der einen Seite das statische Magnetfeld B0 geringfügig verstärken und auf der anderen Seite minimal schwächen, dadurch gehört zur jeder Schicht eine eigene Lamorfrequenz . Diese muss entsprechend durch den HF-Anregungs-Puls geschaltet werden, da sonst die Resonanzbedingung nicht erfüllt ist.
Der Grund für den „Krach“ bei der Kernspintomographie liegt genau hier begründet: in einem stromdurchflossenem Leiter wirkt eine mechanische Kraft (die sog. Lorentzkraft ), dabei verformen sich die Gradientenspulen und knallen auf die umliegenden Bauteile. Die Gradientenspulen sind zwischen dem Hauptmagneten und dem HF-System eingebettet.
6.1.9 Schichtdicke
Die Schichtdicke ist als Ergebnis der Bandbreite des gesendeten HF-Pulses und der Gradienten-Amplitude definiert (Abb. 6.11). Wenn man die Schichtdicke verändern will, muss man entsprechend die Amplitude erhöhen, dabei bleibt die Bandbreite des HF-Pulses gleich.

Abb. 6.11
Schichtselektionsgradient und Schichtdicke
6.1.10 Ortskodierung
Wir haben jetzt eine Schicht angeregt, aber wie entsteht ein Bild in der Kernspintomographie? In der Kernspintomographie besteht eine Schicht aus einzelnen Volumenelementen, auch als Voxel bezeichnet. Am Computer wird das Bild, bestehend aus den verschiedenen Volumenelementen, als Pixelbild dargestellt. Die einzelnen Pixel werden als Rasterbild, wiederum bestehend aus n-Spalten und n-Zeilen, abgebildet. Bei einer Bildmatrix von 4 × 4 reden wir also von 4 Spalten und 4 Zeilen (Abb. 6.12).
Abb. 6.12
Rasterbild von 4 Spalten (Frequenz) und 4 Zeilen (Phasen)
Um jetzt die aus der angeregten Schicht resultierenden Informationen räumlich zuordnen zu können, müssen zwei weitere Gradienten-Schaltungen erzeugt werden:
Phasenkodiergradient , der genau zwischen Anregung und Messung des Signals geschaltet wird,
Frequenzkodiergradient , welcher während der Messung des Signals geschaltet wird.
Das Schalten der unterschiedlichen Gradienten wird am besten anhand eines Beispiels erklärt. Gehen wir davon aus, eine transversale Schicht scannen zu wollen, somit wird ein Schichtselektionsgradient entsprechend der Schichtdicke in z-Richtung zeitgleich mit dem HF-Anregungspuls geschaltet (Abb. 6.13). Wir haben jetzt eine Schicht angeregt, in der alle Spins die gleiche Phasenlage und Frequenz haben.

Abb. 6.13
Schichtselektionsgradient und Schichtdicke in z-Richtung
Um in Phasenkodierrichtung eine räumliche Zuordnung bekommen zu können, müssen wir in Phasenkodierrichtung einen Gradienten schalten. Der bewirkt, dass die Spins in Phasenkodierrichtung unterschiedlich schnell präzedieren, während man den Gradienten schaltet. Sobald der Gradient ausgeschaltet wird, präzedieren alle Spins wieder mit gleicher Frequenz – allerdings mit unterschiedlicher Phasenlage (Abb. 6.14). Dieser Vorgang muss entsprechend der Bildmatrix n-mal wiederholt werden. Bei einer Bildmatrix von 512 muss der Vorgang also 512 x wiederholt werden.
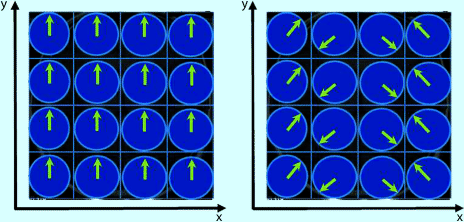
Abb. 6.14
Nach dem Schichtselektionsgradient haben alle Spins die gleiche Phasenlage (links). Der Phasenkodiergradient bewirkt, dass die Spins in Phasenkodierrichtung unterschiedliche Phasenlagen haben (rechts)
Nun schaltet man während des Signalauslesevorgangs den Frequenzkodiergradienten senkrecht zum Phasenkodiergradienten – in unseren Beispiel in y-Richtung (Abb. 6.15). Dadurch präzedieren alle Spins mit unterschiedlicher Frequenz in Frequenzkodierrichtung.
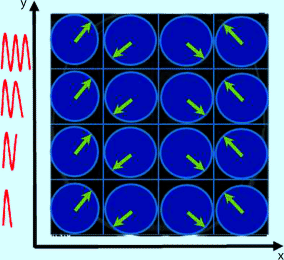
Abb. 6.15
Frequenzkodiergradient in y-Richtung
6.1.11 K-Raum
Die so empfangenen Daten werden im sog. „K-Raum “ gespeichert. Jede einzelne Zeile im K-Raum entspricht einer Messung des Phasenkodiergradienten. Der K-Raum wird Schritt für Schritt gefüllt, dabei enthält jeder Rohdatenpixel Informationen über das gesamte Bild. In der K-Raummitte werden die Kontrastinformationen gespeichert und die außen gelegenen K-Raumzeilen beinhalten die Informationen über die räumliche Auflösung. Mittels der Fourier-Transformation , einem mathematischen Verfahren, wird ein Bild berechnet. Die Fourier-Transformation kennen Sie eventuell noch aus Ihrem Physikunterricht aus dem Bereich der Optik, wo in einem Prisma einfallendes Licht in seine spektralen Anteile bzw. Frequenzen zerlegt wird.
6.1.12 Sequenz
Sie haben in den ersten Seiten jetzt viele neue Informationen bekommen. Lassen Sie uns anhand eines praktischen Beispiels diese einmal zusammenfassen und sortieren:
1.
Ein Patient kommt in den Scannerraum und legt sich auf die Untersuchungsliege.
2.
Dabei richten sich die Wasserstoffprotonen (Spins) zum einen antiparallel und zum anderen parallel entlang des äußeren Magnetfeld B0 aus.
3.
Es richten sich geringfügig mehr Spins parallel aus, daraus entsteht die Longitudinalmagnetisierung Mz.
4.
Außerdem fangen die Spins an zu präzedieren, dies steht in direkter Abhängigkeit zur Magnetfeldstärke.
5.
Als MTRA gehen Sie jetzt an Ihre Bedienkonsole und starten eine Sequenz – in unserem Beispiel eine transversale Sequenz.
6.
Zeitgleich mit dem 90° Anregungspuls wird ein Schichtselektionsgradient geschaltet.
7.
Die Spins werden somit von der Longitudinalmagnetisierung MZ in die Transversalmagnetisierung MXY ausgelenkt.
8.
Die Empfangsspule erhält das erste Signal, bekannt als „Freier Induktionsabfall Signal “ (FID).
9.
Dieses Signal wird nicht für die Bildgebung verwendet.
10.
Danach werden die Phasenkodiergradienten für die Ortskodierung MY geschaltet.
11.
Zum Refokussieren der Spins wird genau zwischen dem 90° Anregungspuls und dem Auslesen des Signals, ein 180°-HF-Puls geschaltet.
12.
Dies geschieht zeitgleich mit einem weiteren Schichtselektionsgradienten, um nur die Spins in der angeregten Schicht kippen zu lassen.
13.
Zum Schluss wird jetzt, während das Signal ausgelesen wird, ein Frequenzkodiergradient geschaltet, um dem Signal eine räumliche Zuordnung in Mx geben zu können.
Herzlichen Glückwunsch: Sie haben soeben Ihre erste Sequenz kennengelernt – eine Spin-Echo-Sequenz (Abb. 6.16).
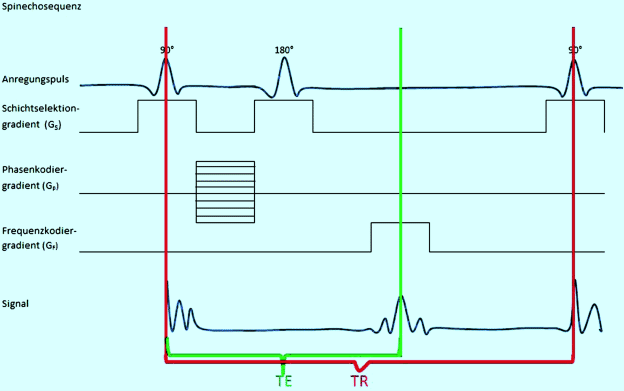
Abb. 6.16
Pulsdiagramm einer Spin-Echo-Sequenz
6.1.13 Repetitionszeit TR und Echozeit TE
Die Repetitionszeit (TR, „T“ für time) ist die Zeit zwischen zwei 90° Anregungsimpulsen. Die TR ist für den Kontrast besonders wichtig, denn je mehr Zeit zwischen den einzelnen Anregungspulsen verstreicht, desto stärker baut sich die Longitudinalmagnetisierung Mz wieder auf. Je mehr Spins wieder in der Longitudinalmagnetisierung Mz bei dem Anregungsimpuls zur Verfügung stehen, umso mehr Signal bekommt man. Jedes Gewebe braucht unterschiedlich lang, um wieder in die Longitudinalmagnetisierung zurückzukehren.
Wenn jetzt der nächste Anregungspuls so geschaltet wird, dass ein Gewebe noch nicht zurück in die Longitudinalmagnetisierung Mz zurückgegangen ist, wird es nach dem nächsten Anregungspuls kaum Signal geben. Man erhält ein eher T1-gewichtetes Bild.
Lässt man stattdessen so viel Zeit (TR) zwischen den Anregungspulsen, dass alle Spins wieder in der Longitudinalmagnetisierung Mz sind, erhält man ein weniger stark T1-gewichtetes Bild.
Die Echozeit (TE) ist definiert als die Zeit zwischen Anregung und maximalem Signalempfangs. Mit der TE können wir den T2-Kontrast eines Bildes beeinflussen. Wählt man eine kurze TE, so bekommen wir ein wenig T2-gewichtetes Bild, weil die Signalintensitäten der verschiedenen Gewebearten noch gering ausfallen.
Wählt man eine längere TE, verstärkt sich die T2-Gewichtung, da Gewebe mit kurzen TE-Zeiten ihr Signal bereits abgegeben haben und nur noch Gewebe mit langer TE zur Kontrastierung beiträgt.
Kontrast
Es gibt in der MRT drei verschiedene Kontraste . Eigentlich spricht man von Wichtung, da ein reines T1- bzw. T2-Kontrastbild kaum möglich ist. Dabei ist die Protonen-gewichtete Sequenz eine Mischung aus vielen Signalen, da lange zwischen den Anregungspulsen (TR lang) und geringer Signalintensität gewartet und die TE kurz gewählt wird (Abb. 6.17).
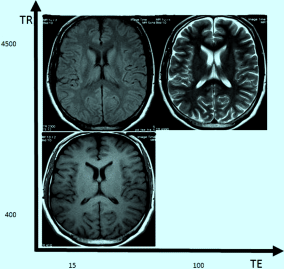
Abb. 6.17
Schema TR-TE-Beziehung mit unterschiedlichen Kontrastbildern
T1-Wichtung mit kurzem TR und kurzem TE (z. B. TR-500 und TE-12)
PD-Wichtung (Protonen-Dichte-Wichtung) mit langem TR und kurzem TE (z. B. TR-2000 und TE-12)
T2-Wichtung mit langem TR und langem TE (z. B. TR-4000 und TE-80)
6.2 Aufbau eines Kernspintomographen
Ein Kernspintomograph hat folgende Hardware Komponenten (Abb. 6.18):

Abb. 6.18
Bild eines Kernspintomographen ohne Verkleidung
Hauptmagnet
Gradientenspulen
Hochfrequenzsystem
Bedienungskonsole und Bildrechner
6.2.1 Hauptmagnet
Der Hauptmagnet erzeugt das statische Magnetfeld B0. Er hat die Aufgabe, ein homogenes Feld zu erzeugen und darf keine bzw. nur geringe Magnetfeldinhomogenitäten unter 5 ppm im Untersuchungsbereich zulassen. Mithilfe von sog. Shimspulen werden etwaige Magnetfeldinhomogenitäten korrigiert. Um die Umgebung vor dem Magneten zu schützen, muss dieser abgeschirmt werden. Heutzutage geschieht dies durch Magnete mit integrierter Abschirmung; dabei handelt es sich um eine doppelte Magnetspule, bei der die innere das Feld erzeugt und die äußere die Magnetfeldlinien zurückführt.
Die heutzutage verwendeten Magnetfeldstärken liegen zwischen 0,1–3,0 Tesla.
Es gibt 3 verschiedene Magnetfeldtypen:
1.
Permanentmagnet
2.
Elektromagnet
3.
supraleitender Magnet
Permanentmagnet
Permanentmagnet e können eine Feldstärke bis 0,5 Tesla erzeugen. Das Magnetfeld verläuft senkrecht zum Patienten. Ein Permanentmagnet kann nicht ausgeschaltet werden. Ein großer Nachteil ist das hohe Gewicht eines solchen Magneten (um die 14 Tonnen) und dass die Homogenität stark temperaturabhängig ist. Allerdings hat ein Kernspintomograph mit Permanentmagnet ein geringes Streufeld und nur geringe Unterhaltkosten.
Elektromagnet
Elektromagnet e können eine Feldstärke bis 0,3 Tesla erzeugen. Das Magnetfeld kann sowohl senkrecht, als auch parallel zum Patienten verlaufen. Die Elektromagnete können abgeschaltet werden. Der Nachteil von Elektromagneten sind der hohe Strom- und Wasserverbrauch. Allerdings hat ein entsprechend ausgestatteter Kernspintomograph ein geringes Streufeld.
Supraleitender Magnet
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree